온라인 차병원보는 세계적으로 권위 있는 SCI(Science Citation Index)급 학술지에 게재된 우수 논문 중 연구실적과 논문 인용 지수, 연구 기여도 등을 폭넓게 고려해 엄선한 논문을 매달 한 건씩 소개합니다. 이달에 소개할 논문은 2025년 01월 국제 학술지 에 실린 차 의과학대학교 약학대학 서영거 교수 연구팀의 논문 ‘TM4SF5와 SLAMF7 결합을 억제하는 isoxazole 기반 약물을 통한 NK세포의 세포독성 회복 및 간암 억제’(IF:40.8)입니다.
간암의 높은 발병률과 낮은 생존율, 효과적인 치료제 개발의 필요성
한국에서 간암 발병률은 여전히 높은 수준이다. 5년 생존율이 39%에 불과해 치명적인 질환으로 간주된다. 최근 면역관문 억제를 기반으로 한 항암제들이 속속 개발되고 있지만, 간암 치료에서는 아직까지 근본적인 한계를 보인다.
이에 차 의과학대학교 약학대학 서영거 교수 연구팀은 서울대학교 약학대학 이정원 교수 연구팀과 공동 연구를 통해, 간암 조직의 상피세포에서 발현되는 막 단백질 TMF4SF5가 NK(자연살상)세포 기능을 억제하는 기전을 밝혀내고, 이를 차단하는 치료제를 개발함으로써 간암 치료의 새로운 가능성을 제시하였다.
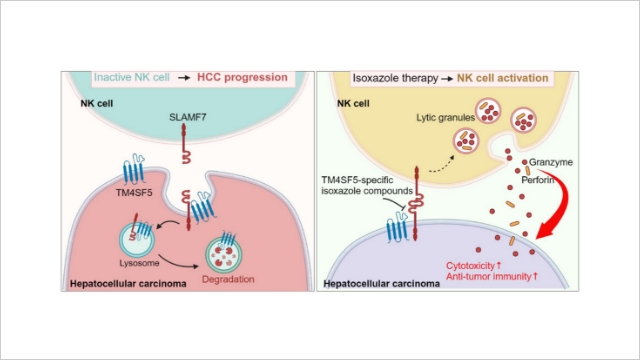
그림 1. (왼쪽) 간암 조직의 ‘TM4SF5 단백질’이 NK세포 활성을 억제하는 기전을 나타낸 그림. 간 상피세포에서 과발현된 TM4SF5는 SLAMF7과 결합하여 이를 세포 내부의 리소좀으로 끌어와 분해한다. SLAMF7이 분해되면 NK세포 활성화가 차단된다. (오른쪽) ‘TM4SF5-특이적 억제 약물(TSI)’을 처리하면, TM4SF5와 SLAMF7의 결합이 차단되어, SLAMF7이 리소좀으로 이동하지 않고 NK세포 또한 활성화되면서 간암 유발이 저하된다.
TM4SF5-SLAMF7 결합을 차단하여 NK세포를 활성화하다
연구팀은 TM4SF5 단백질이 과 발현된 간암 조직에서는 NK세포의 기능이 저하된다는 기존 연구 결과를 주목했다. 이를 바탕으로 연구진은 TM4SF5와 SLAMF7의 결합을 차단하는 신규 저분자 억제제를 개발하였다. Isoxazole 화합물 기반의 ‘TM4SF5 특이적 저분자 억제제(TMF4SF5-specific isoxazole-based small molecules, 이하 TSI)’가 바로 그것으로, 이는 SLAMF7이 리소좀에서 분해되는 것을 막는 역할을 한다. 이 저분자 억제제를 처리하면 NK세포는 항암 기능을 유지해 간암 세포의 성장을 억제하는데, 연구팀은 환자 유래 암 조직 이종이식(PDX) 모델로 이 효과를 확인했다.(그림 2 참고)
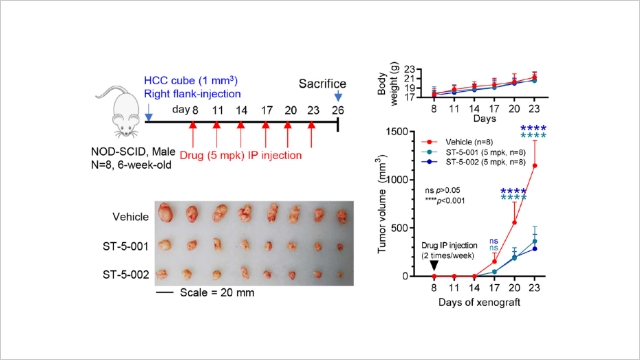
그림 2. 연구팀은 TM4SF5-양성 환자 유래 암 조직 이종이식(PDX) 모델을 활용해 실험을 진행했다. 그 결과 신규 저분자 화합물인 TSI(ST-5-001 및 ST-5-002)를 처리했을 때 체중 감소 없이 종양이 유의미하게 덜 발달한다는 것을 확인할 수 있었다.
효율적인 간암 치료를 위한 새로운 면역관문 억제 전략 제시
연구팀은 이번 연구를 통해, TM4SF5-SLAMF7 축을 표적으로 하여 항암 효과를 유도할 수 있음을 입증하였다. 뿐만 아니라, 발암 물질 처리를 통한 간암 유도, 이종이식 및 환자 유래 암 조직 이종이식(PDX) 등 다양한 간암 동물 모델을 이용하여 TSI의 간암 억제 효능을 검증하였다. 이번 연구는 간암 조직에서 NK세포 활성 조절 기전을 규명하고, 이를 표적으로 한 새로운 패러다임의 면역 항암제 개발 가능성을 제시했다는 점에서 중요한 의의를 갖는다. 차 의과학대학교 서영거 교수 연구팀은 지속적인 연구를 통해 간암 신약 후보 물질 개발에 도전하고 있다.